화이자, 코로나19 경구용 치료제 긴급사용 승인 신청
자체 임상결과, 입원·사망 확률 89%↓..."겨울철 보건당국 대응 도움"
추민선 기자
| cms@newsprime.co.kr |
2021.11.17 09:35:58
[프라임경제] 미국 제약사 머크애드컴퍼니(MSD)의 코로나19 경구용 치료제 긴급사용 승인 신청에 이어 화이자도 미 식품의약청(FDA)에 코로나19 경구형 치료제 긴급사용 승인을 신청했다. 화이자의 경구용 치료제가 FDA의 승인을 받으면 겨울철 코로나19가 재확산할 경우 보건당국의 대응에 상당한 도움을 줄 것으로 보인다.
화이자는 16일(현지시각) 자사가 개발한 코로나19 먹는 치료제 '팍스로비드(Paxlovid)에 대한 긴급 사용을 신청했다고 CNBC가 보도했다.
앨버트 불라 화이자 최고경영자(CEO)는 성명을 통해 "이 잠재적인 치료제를 환자에게 가능한 빨리 제공할 수 있도록 노력하고 있다"며 "우리는 FDA 및 다른 전 세계 규제당국(승인기관)과 협력해 이 신청서를 검토할 수 있기를 기대한다"고 말했다.
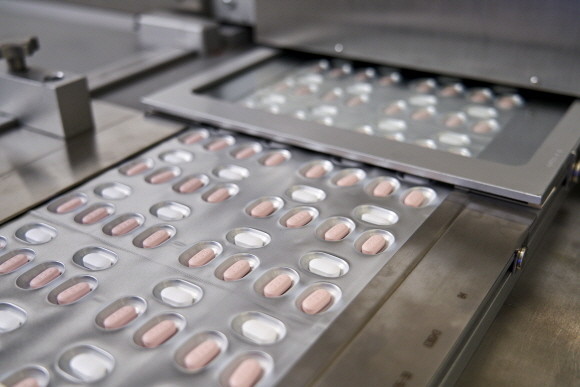
미국 제약사 화이자가 식품의약청(FDA)에 코로나19 경구형 치료제 긴급사용 승인을 신청했다. © 연합뉴스
팍슬로비드가 FDA로부터 긴급사용 승인을 받으면 미국에서 가장 먼저 사용되는 치료제가 될 전망이다. 앞서 지난달 11일 머크는 코로나19 경구형 치료제 '몰누피라비르'의 긴급사용 승인은 신청했지만, 아직까지 결론이 나지 않은 상태다. 영국은 지난 4월 물누피라비르 긴급사용을 승인했다.
팍스로비드라는 이름의 이 코로나19 치료제는 알약 형태의 경구용 항바이러스제로, 자체 임상시험 결과 입원과 사망 확률을 89%까지 줄이는 것으로 나타났다.
팍스로비드가 FDA의 승인을 받으면 미국에서 처음으로 코로나19 치료를 위해 사용되는 경구용 항바이러스제가 될 전망이라고 CNBC방송이 전했다.
FDA 외부 자문단은 오는 30일 만나 치료제의 복용 대상, 사용 방법 등을 결정할 예정이다. 미국 보건당국은 구체적으로 화이자의 신청을 언제 받아들일지 밝히지 않았지만, 적어도 연말까진 승인이 내려질 것이라고 로이터는 전망했다.
ⓒ 프라임경제(http://www.newsprime.co.kr) 무단전재 및 재배포금지



























![[포토] 'AI 공존' TCK '2026 인사이트 포럼'](https://www.newsprime.co.kr//data/cache/public/photos/cdn/20260311/art_726964_1773380545_245x140.jpg)





